|
|
Maslačak(Taraxacum officinale Web.) je trajna, vrlo raširena
biljka čiji se oblik uvelike mijenja prema staništu
i ekološkim uvjetima. Raste na svim kontinentima i nadmorskim
visinama [1,2]. Iako se maslačak često smatra korovom,
radi se zapravo o korisnoj i ljekovitoj biljci. Njegovu ljekovitost
prvi je opisao Hieronymus Bock [3]. Korijen maslačka upotrebljava
se za liječenje raznih bolesti kao što su reuma, giht,
šećerna bolest, bolesti jetre, bubrega i slezene, jer
dobro utječe na vezivno tkivo koje je zbog njegova djelovanja
bolje prokrvljeno, a spriječava i nastanak žučnih
kamenaca [2]. Upotrebljava se u narodnoj medicini kao laksativ,
tonik i diuretik zbog prisustva kalija [4]. Cvjetni pupoljci maslačka
kisele se u octu, služe kao začin ili za pripremu meda.
Mladi listovi koriste se kao proljetna salata još od 17. st.,
a u novije vrijeme maslačak se počeo i uzgajati. Kulturom
je dobiveno nekoliko oblika s velikim listovima. Maslačak
cvate od ožujka do svibnja [2]. Listovi se beru u proljeće,
u travnju i svibnju, a korijen u jesen jer tada sadrži najviše
inulina [5].
Tablica 1: Sadržaj korijena maslačkaa,b
|
Sastojci
|
Masa,
g/kg
|
|
Sastojci
|
Masa,
g/kg
|
|
Sastojci
|
Masa,
g/kg
|
|
inulin
|
400
|
saharoza
|
11
|
fosfor
|
3,6
|
|
bjelančevine
|
165
|
kalcij
|
6,1
|
magnezij
|
2,5
|
|
pektin
|
78
|
natrij
|
5,2
|
vitamin
C
|
0,4
|
|
kalij
|
75
|
glukoza
|
5,0
|
b-karoten
|
0,1
|
|
masti
|
16
|
|
|
|
|
|
a
također su nađeni u manjim količinama: tanini, eterična
ulja, kolin, levulin i gorki heterozidi (taraksacin i taraksacerin);
b navedene vrijednosti su maksimalne
Maslačak je, uz cikoriju, karakterističan predstavnik
porodice glavočika kod kojih su rezervni šećeri
fruktani. Fruktani spadaju u skupinu nestrukturnih energetskih ugljikohidrata
[6]. Prvi ih je opisao njemački znanstvenik Rose (1804.),
a Thomson ih je 1818. godine nazvao inulinom. Osnovna je struktura
fruktana molekula glukoze povezana s mnogo molekula fruktoze (do
200). Fruktane dijelimo na tri skupine: inulini, levani i fruktani
mješovitog tipa, a razlikuju se međusobno po glikozidnim
vezama među molekulama fruktoze. Nama najzanimljivija skupina
su inulini. To su linearni fruktani kod kojih su molekule fruktoze
povezane b(2 -> 1) glikozidnom vezom. Najkraći fruktan inulinskog
tipa je 1-kestoza u kojoj je molekula glukoze povezana s dvije molekule
fruktoze (Slika 1).
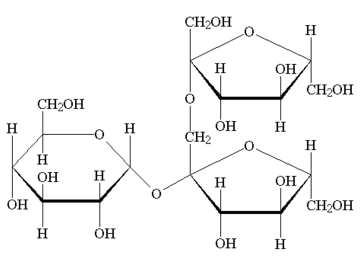
Slika 1: Struktura 1-kestoze
|
 |
|
Tijekom rada korišten je pribor: kuhinjski nož, sušionik, ribež,
porculanska posuda, Erlenmeyerova tikvica, gumeni čep, odmjerna
tikvica, čaša, lijevak, naborani filter papir, mikrovalna peć (snaga
1100 W), sinter lijevak, vodena kupelj, plamenik, univerzalni indikator
papir (Merck), hladnjak.
Upotrijebljene su sljedeće kemikalije: jodna voda (0,1 g joda u
10 cm3 70% etanola); klorovodična kiselina,
HCl (c = 1 mol/dm3 i konc.); natrijev
hidroksid, NaOH (c = 2 mol/dm3); aktivni
ugljen; etanol, C2H5OH
(apsolutni, 96% i 70%); natrijev karbonat, Na2CO3
(c = 1,6x10-6 mol/dm3, pH = 8.5);
vodikov peroksid, H2O2
(w = 28-32%); rezorcinol (1,3-benzendiol), C6H4O2;
fruktoza, C6H12O6.
|
 |
Cilj rada
U okviru ovog rada biti će diskutirana izolacija saharida
iz korijena maslačka. Korijen maslačka je bran u jesen,
jer tada sadrži najviše inulina (čak do 40 %),
[5]. Hidrolizom s klorovodičnom kiselinom i mikrovalnim zagrijavanjem
biti će provedena izolacija inulina u obliku monomera fruktoze.
Također će biti opisana izolacija inulina hidrolizom s
natrijevim karbonatom.
Sakupljanje korijena maslačka
Ubrano je petnaestak korijena maslačka zajedno s lisnom
rozetom, jer se odvajanjem rozete od svježeg korijena gubi
inulin kojeg najviše ima u vrhu korijena, pri lisnoj rozeti.
Za kvalitetniju izolaciju fruktoze i inulina važno je pažljivo
posušiti korijenje maslačka, koje je zajedno s lisnom
rozetom sušeno tjedan dana u prozračnoj prostoriji i
još četiri dana u sušioniku na temperaturi od 45
°C [2]. Lisna rozeta je odrezana (Slika 2). Presjek korijenja
maslačka ovlažen je jodnom vodom pri čemu nije
poplavio, što je dokaz da maslačak ne sadrži glukozu
u obliku škroba [5]. Korijenje je naribano u porculansku posudu.
Dobiveno je 25 g osušenog i usitnjenog korijenja maslačka,
uzorak 1 (Slika 3).
|
|
 |
|
Slika 2: Ubrano korijenje
maslačka
|
Slika 3: Osušeno
i usitnjeno korijenje maslačka, uzorak 1
|
Izolacija fruktoze kiselom hidrolizom
U Erlenmeyerovu tikvicu stavljeno je 8 g uzorka 1 i zakiseljeno
s 20 cm3 klorovodične kiseline
(c = 1 mol/dm3). Tikvica je začepljena
gumenim čepom. Hidroliza je trajala tjedan dana pri temperaturi
37-40 °C u termostatiranom sušioniku. Nakon toga, je sadržaj
tikvice neutraliziran dodavanjem otopine natrijeva hidroksida (c
= 2 mol/dm3), te mu je dodano 20 cm3
destilirane vode. Da je otopina neutralizirana, potvrđeno je
univerzalnim indikator papirom. Uzorak je profiltriran preko naboranog
filter papira da bi se uklonili ostaci staničevine, a filtrat
mikrovalno zagrijavan 1 minutu u kuhinjskoj mikrovalnoj pećnici.
Filtrat je bio mirisa meda i izrazito žute boje. Nakon toga
uzorak je profiltriran preko sinter lijevka i pročišćen
nekoliko puta aktivnim ugljenom, uz zagrijavanje na vodenoj kupelji
pri temperaturi 95 °C (Slika 4). Aktivni ugljen odvojen
je filtracijom, a filtrat je pažljivo uparen na vodenoj kupelji
do suhoga tako da fruktoza ne karbonizira. Prekristalizacija je
izvedena najprije iz apsolutnog, a potom iz 96% etanola. Dobiveni
su smeđi higroskopni kristalići izoliranog materijala
2 (Slika 5), m = 1,57 g, (19,6%).
|
|
 |
|
Slika 4: Pročišćavanje
aktivnim ugljenom
|
5: Izolirani materijal
2
|
Izolacija inulina u baznom mediju
U Erlenmeyerovu tikvicu stavljeno je 6,2 g uzorka 1 te zaluženo
sa 100 cm3 otopine natrijeva karbonata,
(c = 1,6x10-6 mol/dm3, pH = 8.5). Izluživanje
je trajalo 1 sat pri temperaturi od 60 °C u termostatiranom
sušioniku. Nakon izluživanja, sadržaj tikvice filtriran
je preko naboranog filter papira da se uklone mehaničke nečistoće.
Filtrat je bio izrazito smeđe boje. Uzorku, ohlađenom na
20 °C, dodaje se 50 cm3 vodikova
peroksida (w = 28-32%). Dolazi do intenzivnog pjenjenja tijekom
2,5 sata zbog relativno visokog udjela proteina (36-165 g/kg). Vodikov
peroksid oksidira nečistoće ekstrahirane iz korijena
maslačka zajedno s inulinom, ali ne može oksidirati
hidroksilne skupine inulina [7]. Filtrat nakon dodatka vodikova
peroksida mijenja boju do bistro žute. Nakon prestanka pjenjenja,
reakcijska smjesa spremljena je u hladnjak na temperaturu od 4 °C
pri čemu su dobiveni kristali 3.
Analiza izoliranog materijala
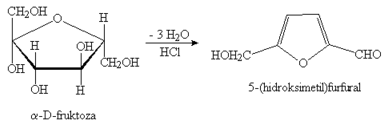
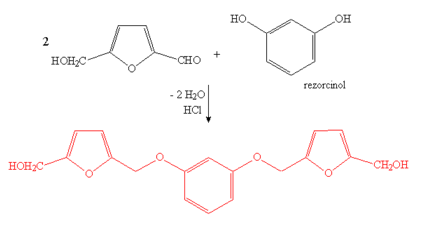
Prisustvo ketoza (fruktoze) može se dokazati Seliffanovljevim
reagensom, koji se dobiva otapanjem rezorcinola (1,3-benzendiola)
u razrijeđenoj klorovodičnoj kiselini. Prilikom dodatka
ovog reagesa otopini ketoze klorovodična kiselina oduzima
tri molekule vode, pri čemu nastaje derivat furfurala koji
s rezorcinolom stvara kondenzacijski produkt crvene boje, (Shema
1).
Shema 1
 Seliffanovljev
reagens pripremljen je otapanjem 1 g rezorcinola u destiliranoj
vodi kojoj je dodano 33 cm3 konc. klorovodične
kiseline, te je razrijeđena do 100 cm3
u odmjernoj tikvici [8]. Vodena otopina izoliranog materijala 2
dodatkom Seliffanovljevog reagensa daje crveno obojenje, a isti
rezultat je dobiven dodatkom reagensa u vodenu otopinu izoliranog
materijala 3. Kao slijepa proba, reagens je dodan u otopinu
fruktoze (p.a.) koja se također obojila u crveno. Seliffanovljev
reagens pripremljen je otapanjem 1 g rezorcinola u destiliranoj
vodi kojoj je dodano 33 cm3 konc. klorovodične
kiseline, te je razrijeđena do 100 cm3
u odmjernoj tikvici [8]. Vodena otopina izoliranog materijala 2
dodatkom Seliffanovljevog reagensa daje crveno obojenje, a isti
rezultat je dobiven dodatkom reagensa u vodenu otopinu izoliranog
materijala 3. Kao slijepa proba, reagens je dodan u otopinu
fruktoze (p.a.) koja se također obojila u crveno.
|
 |
|
Ubran je korijen maslačka u jesen, kada sadrži do 40% inulina,
te je sušen i usitnjen. Njegovom kiselom hidrolizom (HCl, c = 0,1
mol/dm3) te prekristalizacijom iz etanola
izoliran je materijal 2, a izlučiavnjem (Na2CO3,
c = 1,6x10-6 mol/dm3,
pH = 8.5) je dobiven materijal 3. Analiza Seliffanovljevim
reagensom je pokazala da uzorci 2 i 3 sadrže ketoze.
|
 |
|
- Nikolić (ur.),
Liječnik u kući,
Stvarnost, Zagreb, 1971, str. 467-468
- Lj. Grlić,
Enciklopedija samoniklog jestivog bilja,
August Cesarec, Zagreb, 1986, str. 325-327
- R. Willfort,
Ljekovito bilje i njegova upotreba,
Mladost, Zagreb, 1989, str. 371-372
- http://www.mc.vanderbilt.edu/vumcdept/derm/contact/TA001.html
- J. Tucakov,
Lečenje biljem,
Rad, Beograd, 1986, str. 469-471
- http://www.geocities.com/CapeCanaveral/4409/fructan.htm
- Cristianio Pedersini, Polytech S.c.a.r.l. Area Science Park,
Padriciano 99, 34012 Trieste, Italy
(diskusijska lista za prirodne spojeve na Internetu: napronet@bilkent.edu.tr)
- A. Kučak,
Vježbe iz organske kemije i biokemije,
Interna skripta, Rudarska i kemijska
škola, Varaždin, 1996
- http://hpd.botanic.hr/kem
Zahvala
E-školi mladih znanstvenika
(9) na financijskoj potpori te
dr. sc. Cristianu Pedersiniju,
Politech (Trst),
recenzentici mr. sc. Ivanki Jerić,
Institut "Ruđer Bošković"; (Zagreb) i
lektorici prof. Vesni Marković,
Rudarska i kemijska škola (Varaždin) na savjetima i diskusijama.
|
|

|