|
 |
|
molim vas da mi objasnite na molekularnoj razini zašto kristali za razliku od amorfnih tvari imaju odredjenu temperaturu taišta, a amorfne tvari ne.Hvala unaprijed.
|
|
Ime i prezime:
ivana trogrlić
Anto.Trogrlic@public.srce.hr
|
 |
 |
Svaki dio unutrašnjosti kristala ima potpuno jednaka fizikalna i kemijska svojstva. Zašto? Pa zato što je građen od istih dijelova - elementarnih ćelija. Cijeli kristal se tali na istoj temperaturi jer je svugdje energija kristalne rešetke jednaka.
Kod amorfnih tvari ne postoji jedinstveni uzorak koji se ponavlja u prostoru poput elementarne ćelije. Negdje su atomi bliže jedni drugome, drugdje su na većim udaljenostima i drugim položajima. Taljenje će početi gdje je vezanje najslabije, zatim će se taliti područja s bolje složenim atomima/molekulama, a tek na kraju će se, ako postoje, raspasti kristalične zone u kojima je slaganje najbolje i energija vezivanja najveća. Stoga taljenje amorfnih tvari teče postupno, a početna temperatura mekšanja je niža od tališta potpuno kristalične tvari istog kemijskog sastava (ovisi i o alotropskoj modifikaciji).
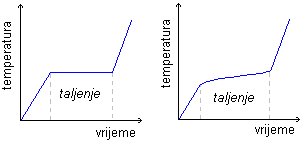
Ovako bi izgledalo taljenje kristala (lijevo) i amorfne tvari (desno). |
|
|
Odgovorio:
Kristijan A. Kovač
kkovac@chem.pmf.hr
<-- Povratak
|
 |
 |
U prethodnom odgovoru, prijatelja i kolege Kristijana, rečeno je da se kristali od amorfnih tvari bitno razlikuju posjedovanjem uređene strukture, jedinični element - elementarna ćelija - ponavlja se u trodimenzionalnom prostoru na određeni način, a sve su ćelije jednako orijentirane pritom. To sve stoji. No, istaknuta druga razlika - među jedinkama (česticama) koje grade amorfnu tvar veze su različite duljine, znači energije, dok su veze među česticama kristala uvijek iste duljine - odakle je onda izveden zaključak o postojanju tališta (ili temperature taljenja; pazi: ne "temperatura tališta" (kako je u tvom pitanju napisano)) u kristala, i nepostojanju istog u amorfnih tvari, jednostavno nije razlika među kristalima i amorfnim tvarima! Jer, i unutar strukture nekog kristala mogu veze biti različite duljine među istim česticama, pa to nije onda razlika, a posebno ne ona koja objašnjava postojanje temperature taljenja u kristala, i nepostojanje iste u amorfnih tvari!! Što je onda pravi odgovor?!
U razmatranju pojave taljenja kristala valja uzeti u obzir sve doprinose u energiji interakcija pojedine čestice s česticama koje ju okružuju u bližoj i daljoj okolini, prije svega u blizini, doprinose u energiji interakcija te čestice s vezama kojima je vezana, neposredno i posredno (tu posebno valja uzeti u obzir, kod molekulskih kristala, vodikove veze, koje su tu najodgovornije za strukturu koja jest) i gledati te doprinose kao prostorno uvjetovane. Za ionske kristale, one vrlo simetrične, poput NaCl, postoji model energije kristalne rešetke, koju kao dio topline taljenja privodimo kristalu pri taljenju, tzv. Born-Mayer-Landeova jednadžba, koja uzima u obzir kulonske interakcije privlačenja i Bornove interakcije odbijanja, i to uzima sve u obzir kao prostorno uvjetovano. No to je jedan od najprimitivnijih modela, i to samo za specifične ionske kristale, čak ne sve ionske, dakle! Modelirati kovalentne ili molekulske kristale daleko je složenije, tu postoji rad ruskog fizičara Aleksandra Isaakoviča Kitajgorodskog koji postavlja energiju rešetke kao sumu svih doprinosa u energijama različitih interakcija po molekuli, za sve molekule, tj. čestice, u kristalu!!! Ipak, tom modelu prigovara se nedovoljna briga o vodikovim interakcijama. Još složeniji modeli izviru iz kvantne fizike (Dirac, Debye)!!!! Kako u amorfnih tvari nema takve organizacije - kompletne - to nema ni sumiranja doprinosa kojih bi sume bile u svakom pojedinom trenutku jednake - time bi u pojedinim trenutcima kristal uzimao uvijek jednake obroke energije, a time bi opet i, s energijom čvrsto povezana, temperatura taljenja u svakom trenutku bila ista, kao što je to kod kristala!!!!! Struktura, ukupno gledajući, uvjetuje (ne)postojanje tališta!!!!!! |
|
|
Odgovorio:
Marko Grba
<-- Povratak
|
 |
 |
Moram se ispričati svima koji su pročitali moj odgovor jer je, priznajem, šlampav. Dogodio mi se lapsus i nehotice sam pomiješao dva vrlo različita pojma - elementarne ćelije i udaljenosti među atomima. Zahvaljujem Marku što je uočio pogrešku i još se jednom ispričavam svima koje sam zaribao. |
|
|
Odgovorio:
Kristijan A. Kovač
kkovac@chem.pmf.hr
<-- Povratak
|
|

|
Postavite
pitanje iz bilo kojeg područja kemije i
e-škola će osigurati da dobijete odgovor od kompetentnog znanstvenika. |
  |
|

