|
 |
|
Voda, cijanovodik i amonijak imaju visoko talište i vrelište, visoku relativnu permitivnost ili dielektričnu konstantu i s time u vezi veliku moć otapanja soli, radi asocijacije vodikovim vezama. Što je relativna permitivnost ili dielektrična konstanta, kako na nju utječe vodikova veza i zašto te tvari dobro otapaju soli?
Pozdrav.
|
|
Ime i prezime:
Tamara Vasilj
tammy_1@net.hr
|
 |
 |
U nekim tvarima (dielektrici, najčešće su izolatori) pod utjecajem vanjskog električnog polja induciraju se dipoli (polarizacija) zbog kojih je efektivna vrijednost jakosti električnog polja manja. Ti dipoli mogu postojati od prije, kao polarne molekule ili atomske skupine, ali koje će se u električnom polju orjentirati odprilike u istom smjeru. Omjer jakosti električnog polja u mediju i vakuumu je relativna permitivnost (prije - dielektrična konstanta), εr. Permitivnost vakuuma je jedna od osnovnih prirodnih konstanti:
ε0 = 8,854·10-12 F m-1 (farad po metru)
Permitivnost nekog sredstva je njihov umnožak (za vakuum εr = 1):
ε = εr ε0
Prema Coulombovu zakonu iznos sile između dva električna naboja q1 i q2 razmaknuta za r je obrnuto razmjeran permitivnosti sredine u kojoj su naboji smješteni:
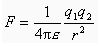
Ako neku tvar na okupu drže elektrostatske sile između suprotno nabijenih čestica, kao što je slučaj s ionskim spojevima, te će se čestice lakše razdvojiti kad se između njih postavi dielektrik, posebno što je veća relativna permitivnost. Sila između dva iona odijeljena vodom je odprilike 80 puta slabija nego u vakuumu. Tvari izrazito polarnih molekula, među koje spada i H2O, obično imaju velike relativne permitivnosti kao što možeš provjeriti u tablici.
Tablica 1. Relativne permitivnosti nekih tvari pri 25 °C.

Nije permitivnost vode tako velika samo zbog dipolnosti molekula. Mreža vodikovih vezâ koja se proteže kroz agregate molekula zapravo je odgovorna za neobična električna svojstva tekuće vode i leda. Povišenjem temperature atomi i molekule se sve više nasumce okreću pa permitivnost opada i to vrijedi za sve tvari. Kod vode dodatno utječe kidanje vodikovih veza na visokim temperaturama. Superkritična voda (zagrijana pod vrlo visokim tlakom iznad kritične temperature) kao otapalo sliči nepolarnim organskim tekućinama jer se relativna permitivnost može spustiti ispod 5.
Tablica 2. Relativne permitivnosti vode pri različitim temperaturama. Negativne temperature odnose se na pothlađenu vodu.

Neke druge tvari se slično ponašaju, uključujući amide iz tablice 1, cianovodik (21 °C, εr = 95) i nešto manje amonijak (-34 °C, εr = 22). |
|
|
Odgovorio:
Kristijan A. Kovač
kkovac@chem.pmf.hr
<-- Povratak
|
|

|
Postavite
pitanje iz bilo kojeg područja kemije i
e-škola će osigurati da dobijete odgovor od kompetentnog znanstvenika. |
  |
|

