|
 |
|
Na temelju kristalne strukture i gustoće natrijevog klorida te ionskog polumjera natrijevog kationa izračunajte ionski polumjer kloridnog iona.
ρ(NaCl) = 2,165 g cm-3, r(Na+) = 95 pm.
|
|
Ime i prezime:
Lorena Dotur
lorena_si@yahoo.com
|
 |
 |
U natrijevu kloridu ioni su složeni u jednostavnu kubičnu strukturu koju bismo mogli zamisliti kao onu prikazanu na slici 1. Cijeli kristal sastavljen je od jediničnih ćelija (slika 2). U jediničnoj ćeliji su ukupno 4 iona natrija i 4 kloridna aniona. Možda na slici ne izgleda tako, ali ioni u vrhovima kocke pripadaju samo jednom osminom jediničnoj ćeliji, ioni na rubovima četvrtinom, ioni na sredini ploha polovicom.
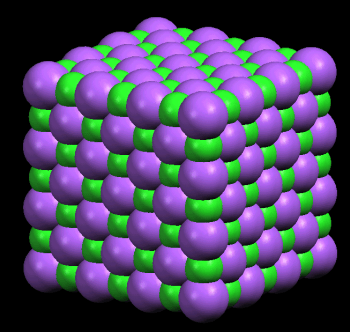
Slika 1. Kristalna struktura natrijeva klorida. Veće kuglice predstavljaju kloridne ione, manje natrijeve.
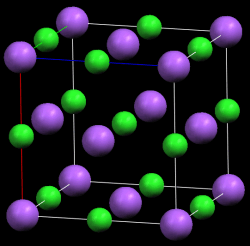
Slika 2. Jedinična ćelija natrijeva klorida.
Zadana gustoća odnosi se jednako na čitav kristal kao i na jediničnu ćeliju. Masa natrijeva klorida sadržana u ćeliji jednaka je zbroju masa po četiri atoma natrija i klora. Volumen je jednak kubu duljine brida kocke a. Dakle
ρ = [4ma(Na) + 4ma(Cl)]/a3
Brid je ujedno povezan s ionskim radijusima (slika 3):
a = 2r(Na+) + 2r(Cl-)
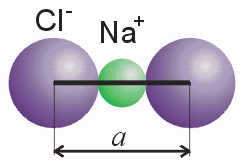
Slika 3. Duljina brida jedinične ćelije.
|
|
|
Odgovorio:
Kristijan A. Kovač
kkovac@chem.pmf.hr
<-- Povratak
|
|

|
Postavite
pitanje iz bilo kojeg područja kemije i
e-škola će osigurati da dobijete odgovor od kompetentnog znanstvenika. |
  |
|

