|
 |
|
Napišite mi broj elementarnih čestica za :
Al,O,Li
|
|
Ime i prezime:
stjepan Kumrić
stjepan.kumrić@vz.htnet.hr
|
 |
 |
Koliko sam razumio, zanima te broj protona, elektrona i neutrona u atomima aluminija, kisika i litija?
Prvo što trebaš je periodični sustav elemenata. Svaki element ima svoj vlastiti redni broj (Z). Atomi različitih elemenata razlikuju se po broju protona u jezgri, počevši od atoma vodika sa samo jednim protonom pa sve do najtežih atoma koji imaju i preko stotinu protona. Broj protona u jezgri jednak je rednom broju elementa u periodičnom sustavu. Izolirani neutralni atom (bez naboja) u elektronskom omotaču ima elektrona koliko i protona, jer inače ne bi bio neutralan:
Z = N(p+) = N(e-)
(Z - redni broj, N(p+) - broj protona, N(e-) - broj elektrona)
Sa neutronima je nešto teže, ali i to se »da srediti«. Broj neutrona u atomu istog elementa razlikuje se od izotopa do izotopa. Npr. vodik - u prirodi postoje dvije vrste atoma vodika. »Običan« vodik (procij, 1H) u jezgri nema neutrona, samo jedan proton. Jezgra težeg izotopa, deuterija (2H) ima uz proton i jedan neutron. Postoji i još teži izotop, tricij (3H), sa dva neutrona u jezgri atoma.
Zbroj protona i neutrona u jezgri naziva se masenim brojem (A):
A = N(p+) + N(n0)
Maseni brojevi izotopa pišu se uz simbol elementa s gornje lijeve strane (kao u primjerima s izotopima vodika).
Ako znamo maseni broj nekog atoma, lako ćemo izračunati broj neutrona. No, trebamo znati i o kojem se izotopu radi. Elementi se u prirodi javljaju u više izotopa. Za početak ćemo pogađati kojeg izotopa u prirodi ima najviše. U periodičnom sustavu uz redne brojeve elemenata nalazimo i njihove relativne atomske mase (Ar). Te mase nisu cijeli brojevi. Relativna atomska masa kisika je 15,9994, obično zaokružena na 16,00. Jedan od razloga zašto ti brojevi nisu cijeli je i postojanje izotopa pa relativna atomska masa izražava prosjek. Ako zaokružimo relativnu atomsku masu na cijeli broj, najčešće ćemo dobiti maseni broj nekog uobičajenog izotopa tog elementa (ali ne uvijek!).
Zaokružimo relativnu atomsku masu kisika na 16 i doista - najčešći izotop kisika u prirodi je kisik 16 (16O). Iz njegova masena broja 16 i rednog broja 8 možeš izračunati broj neutrona u jezgri atoma. Pokušaj isto s aluminijem i litijem. A ovdje je lista izotopa tih elemenata zajedno s masenim udjelom u kojem se javljaju u prirodi u nekom prosječnom uzorku. Možeš izračunati N(p+), N(e-) i N(n0) za svaki od izotopa.
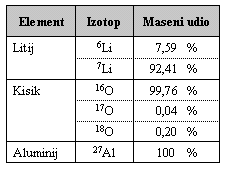
Tablica. Prosječan izotopski sastav litija, kisika i aluminija.
<
Izotopski sastav elemenata možeš pronaći u mnogo izvora, u knjigama kao i na Internetu. Zgodna web-stranica je Table of Nuclides:
http://atom.kaeri.re.kr/ton/main.shtml |
|
|
Odgovorio:
Kristijan A. Kovač
kkovac@chem.pmf.hr
<-- Povratak
|
|

|
Postavite
pitanje iz bilo kojeg područja kemije i
e-škola će osigurati da dobijete odgovor od kompetentnog znanstvenika. |
  |
|

