|
 |
|
kako se može dobiti sapun, a kako deterdžent? Koji su njihovi sastavi, te po ćemu se razlikuju?
|
|
Ime i prezime:
Božica Esapović
besapovi@net.hr
|
 |
 |
I sapuni i deterdženti imaju izdužene molekule kojima je jedan kraj hidrofilan (topljiv u vodi), a drugi hidrofoban (nije topljiv u vodi, odnosno topljiv je u mastima) i djeluju na isti način.
Sapuni su soli karboksilnih kiselina dugog ugljikovodičnog lanca. Takve su više masne kiseline koje su u mastima povezane s glicerolom. Djelovanjem jakih (alkalijskih) lužina masti se razlažu (hidroliziraju) na glicerol i soli masnih kiselina:
- ovo je primjer hidrolize jedne molekule iz masti (tripalmitoilglicerol)
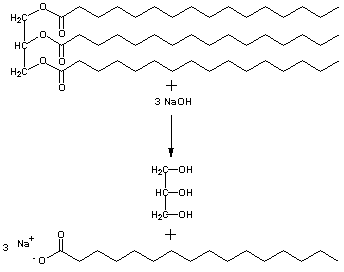
Dio molekule koji nosi naboj (lijevo na slici) je hidrofilan. Natrijev iona nije bitan za sposobnost pranja sapunom. Međutim, ako u vodi ima mnogo kalcija, nastaju kalcijevi sapuni netopljvi u vodi. Pitka voda je obično tvrda (veća koncentracija kalcija) što otežava pranje i povećava utrošak sapuna. S deterdžentima takvih problema uglavnom nema.
Deterdženti nemaju karboksilne hidrofilne skupine. Glavna sirovina su ugljikovodici iz nafte, a dobivanje je puno kompliciranije. Osim što ne reagiraju s kalcijem, deterdženti imaju još nekih prednosti. »Dizajniraju« se prema namjenama, a tu su mogućnosti gotovo neograničene. Npr. po potrebi ne stvaraju pjenu, peru u kiselim otopinama, mogu nositi pozitivni ili negativni naboj ili biti neutralni... Sapuni su izvedeni iz masti pa te spojeve mikroorganizmi vrlo lako razgrađuju kad dospiju u okoliš. S deterdžentima ide teže. Nekada su često imali razgranati hidrofobni ugljikovodični dio, a s time se bakterije moraju posebno pomučiti. Danas je većina deterdženata ipak s ravnim lancem.
Dva »običnija« deterdženta:
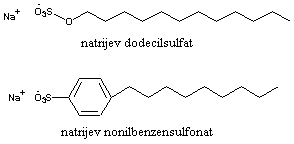 |
|
|
Odgovorio:
Kristijan A. Kovač
kkovac@chem.pmf.hr
<-- Povratak
|
|

|
Postavite
pitanje iz bilo kojeg područja kemije i
e-škola će osigurati da dobijete odgovor od kompetentnog znanstvenika. |
  |
|

